はじめに
近年、日本でも様々な種類のチーズが流通し、消費量も平成2年には15.3万トンであったものが、平成12年には26万トン近くに増加し、その後、ほぼ一定となっている(農林水産省 平成19年度チーズ需給表)。また、この間、ナチュラルチーズの消費量も大きく伸び、国内においても“チーズを食べる”と言う文化が深く浸透してきているといえるが、それでも一人あたりの消費量が最も多いフランスと比較すると消費量は10%程度である。
元来、チーズには良質なタンパク性成分やカルシウムが豊富に含まれており、栄養価が高い食品であることが広く認識されてきた。また、最近になってチーズおよびチーズ成分が持つ保健効果に関する研究が精力的に進められてきたが、ヨーグルトのような他の乳製品に比べ、チーズの保健効果に関しては消費者に広まっていない。もし、チーズに関する種々の新規保健効果の科学的根拠が得られ、消費者に認知されれば、チーズの消費拡大につながるものと考えられる。
これまでに明らかにされてきたチーズの保健効果として、虫歯予防効果、循環器系疾患リスクの低減および肥満抑制効果などが報告されている1)。チーズの虫歯予防効果の作用機序には、チーズに含まれているリン酸カルシウムが、歯のエナメル質の脱灰(歯に穴があくこと)化を減少させることが寄与しているものであり、虫歯原因菌であるStreptococus mutansに対する抗菌活性の関与は低いようである。チーズスターターに用いられる乳酸菌の抗菌物質バクテリオシンに関する研究は数多く報告されている一方で、発酵や熟成の結果、派生してくる抗微生物物質に関する報告はあまり見られない。
本稿では、チーズ成分の生化学的変化の概要を述べるとともに、脂質の化学変化とそれによって生じる遊離脂肪酸の抗微生物作用の可能性について論じる。これらの中で、特に、胃炎、胃・十二指腸潰瘍、胃がん、胃リンパ腫との関連が示唆されているHelicobacter pylori(以下、ピロリ菌という)を取り上げ、筆者らがピロリ菌の自己溶菌現象に関する作用機序の解明を進める中で明らかにしてきた現象をヒントに、チーズの抗ピロリ菌作用を検討してきた結果についても紹介する。
1 チーズ成分の生化学的変化
(1)成分の分解
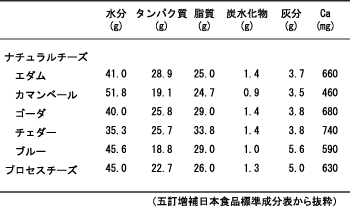
一般にチーズは原料乳に乳酸菌を添加、発酵させ、凝乳酵素を添加し、程よく固まったのち、型に入れて圧搾、場合によっては加塩し、一定湿度および温度で熟成というプロセスを経て製造される。チーズ製造に使用される微生物は、乳酸菌のほか、青カビ(ブルー)チーズに利用されるPenicillium roqueforti、カマンベールのような白カビチーズに利用されるPenicillium camembertiなどが挙げられる。これらの微生物の働きで、チーズ固有の風味を醸し出すとともに、チーズ独特の組織が形成される。表1に、各チーズ類の一般組成を示したが、主成分は、タンパク質と脂質であり、乳酸菌は主にタンパク質を分解し、特有な味や香りなどを作り出す一方、カビ類は、脂肪とタンパク質の分解力が強く、チーズの内部でも生育し、独特の風味と香りを作り出す。このように、チーズの熟成中に起こる成分の生化学的変化で主要なものは、乳タンパク質と脂肪の分解であるといえる。
表1 チーズの主要成分の組成(100gあたり)
(2)乳タンパクの分解
乳タンパク質に関しては、主な成分であるカゼインの分解が極めて重要である。チーズ製造過程において、カゼインは、凝乳酵素レンネット、乳中のプロティナーゼによって電気泳動で検出される程度の高分子ペプチドに分解され、また、乳酸菌や二次スターターのプロティナーゼやエンドペプチダーゼにより、それ以下の低分子ペプチド、さらにはエキソプロテアーゼの作用を受け、アミノ酸へと分解される(図1)。チーズ製造過程のカゼインの分解様式については、他の総説を参照されたい2,3)。
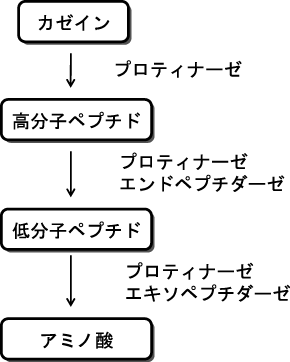
図1 チーズ熟成中のカゼインの分解
(3)脂肪の分解
チーズのもう一つの主成分である脂肪も熟成期間中に分解を受ける。チーズの脂肪の由来は当然のことながら乳由来のものであり、熟成前では乳脂肪を36〜40%含んでいるが、熟成後では30%程度含んでいる。牛乳を例に脂質組成を表2に記した。主要な脂質は、グリセロールの脂肪酸トリエステルであるトリアシルグリセロール(トリグリセリドともいう)であり(図2)、遊離脂肪酸はほとんど含まない。一方、チーズ熟成期間中に、トリアシルグリセロールは、リパーゼの作用を受け、脂肪酸とグリセロールに分解される。熟成期間中の脂肪分解反応は、風味の発現においてきわめて重要な生化学反応である。脂肪酸はカルボキシル基1個を持つカルボン酸のうち鎖状構造を持つものの総称であり、その長さにより、短鎖脂肪酸、中鎖脂肪酸、長鎖脂肪酸に分類される。また、二重結合を持たないものを飽和脂肪酸、一つ持つものを一価不飽和脂肪酸、二つ以上持つものを多価不飽和脂肪酸と呼び、炭素原子数:二重結合数で表記する。
表2 乳脂肪の分類と組成(重量%)

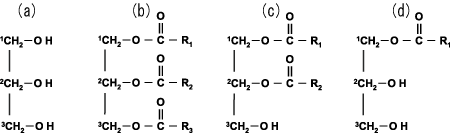
図2 (a)グリセロール、(b)トリアシルグリセロール、
(c)ジアシルグリセロール、(d)モノアシルグリセロールの一般式
(4)遊離脂肪酸と共役リノール酸
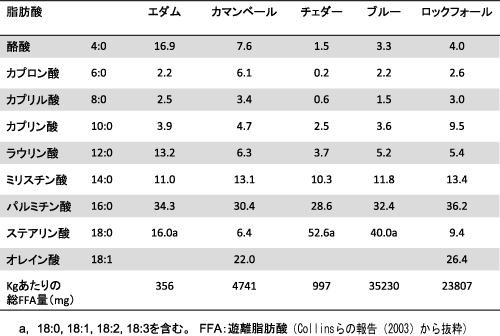
それでは、実際のチーズにどのような遊離脂肪酸が含まれているのであろうか。代表的なチーズに含まれる遊離脂肪酸量を表3に示した。その含量は原料乳の搾乳時期やチーズ製造および熟成条件によって、大きく影響を受けるものである。大まかな傾向としてチェダーやゴーダのような乳酸菌熟成タイプにおいては、遊離脂肪酸含量は低いが、カビを利用した熟成タイプやパルメザンのような長期熟成タイプのチーズにおいて高いことが知られている。総脂肪酸量に対する不飽和脂肪酸は、30〜40%程度占めている。
表3 チーズの脂肪酸組成(総脂肪酸量に対する重量%)
反すう動物で合成される共役リノール酸(Conjugated linoleic acid;CLA)も乳製品に比較的多く含まれる。
CLAは、反すう動物が飼料から摂取したリノール酸をルーメン微生物のリノール酸イソメラーゼの作用によって、水素添加されて生じる中間体として生成される。リノール酸は炭素数18から成り、カルボキシ基の炭素から数えて9位と12位に二重結合が存在するが、この異性体として、9位と11位の2か所に二重結合が存在していることが見出され、二重結合が単結合と交互になっているため、“共役”リノール酸と呼ばれるに至った。CLAはいくつかの異性体を持つが、牛肉や乳製品で見られる75%以上は、シス-9、トランス-11CLA異性体で占められる。
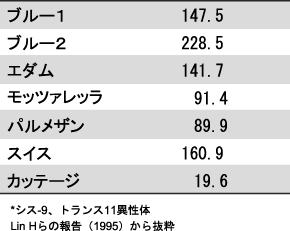
チーズ中のCLA含量は、チーズによって異なるものの、多くのチーズで100gあたり100〜200mg程度含まれる(表4)。なおチーズ中のCLAは飼料に依存するところが大きいが、乳酸菌スターターがCLA合成に関与していることも示唆されている26)。
表4 チーズ中の共役リノール酸*含量(mg/100gサンプル)
2 チーズの脂質に秘められた新規保健機能
(1)CLAの保健機能に期待
近年、食品の機能に関する研究が注目されるようになってから、さまざまな保健機能を持つ成分が発見されてきた1)。食品の中でも乳中には多くの生理活性成分が見出されている。
チーズは、発酵や熟成の過程を経て、乳中成分が質的変化を受けたものであり、栄養成分が濃縮されると同時に、保健機能を持つ成分も濃縮され、新たに派生していることが推察される。特にペプチド成分に関しては、多くの研究が精力的になされており、他の総説を参照いただきたい4,5)。ここでは、チーズの主要成分である脂質成分について期待される保健機能について述べることとする。
前述のCLAの保健機能については、当初、加熱調理されたハンバーガー中から抗変異原性を示す物質として見出されてから、注目されるようになった。これまで、in vitro及びin vivoで報告されてきたCLAの保健機能について表5にまとめた。
表5 CLAの保健機能

チーズ中には、他の乳製品より多くのCLAが含まれていることから、CLAの保健機能を期待するには適した食品といえる。
また、CLA合成能をもつ乳酸菌をチーズスターターとして用いることによって、チーズ中のCLAを強化した新しいタイプのチーズを提供することも可能になるかもしれない。
(2)抗微生物作用について
その他の脂質の保健機能として、抗微生物作用が知られている。すなわち、遊離脂肪酸やモノアシルグリセリドは多くのグラム陽性および陰性細菌、エンベロープウイルスなどに抗微生物作用を示す。これらの効果は、ジグリセリドやトリグリセリドには見られないとの報告もある6)。また、Sunらは、牛乳脂質からリパーゼによって遊離した脂肪酸のグラム陽性菌およびグラム陰性菌に対する抗菌活性を検討したところ、脂肪酸の鎖長によって抗菌活性は異なり、前者に対してはC12:0のラウリン酸が、後者に対してはC8:0のカプリル酸が最も高い抗菌性を示したことを報告した。また、彼らは、牛乳が胃潰瘍の症状を緩和するといった報告と牛乳由来脂肪酸の抗微生物作用を関連付け、牛乳由来の脂質のピロリ菌に対する抗微生物作用を検討した。その結果、カプリン酸、ラウリン酸、ミリスチン酸などの脂肪酸が他の脂肪酸より高い抗菌活性を示すことを見出した7-9)。
これらの結果から、チーズ中に遊離してくる脂肪酸にも抗微生物活性が見出されることが容易に推察されるが、これまで、チーズの脂質成分中の抗微生物活性についてはあまり検討されてこなかった。
一方、後述するが、筆者らは、ピロリ菌が自ら溶菌するという現象を見出してきたが、その過程で細胞膜由来脂質成分が自己溶菌に関与していることを見出してきた。そこで、我々は比較的脂質を含むチーズに着目し、ピロリ菌に対する抗微生物作用に関する検討を進めているので、以下に紹介する。
3 ピロリ菌とその溶菌現象
(1)ピロリ菌と疾患
ピロリ菌は1983年にWarrenとMarshalによって胃の下部から検出、分離培養され10,11)、胃潰瘍や十二指腸潰瘍の原因菌として知られている。本菌が発見された当時、強酸性である胃内には細菌が棲息できるはずがないとの主張がなされ、本菌の胃内での存在自体を否定する研究者も多い状況であった。そこで、Marshalは自ら本菌を飲み、急性胃炎になることや抗生物質で除菌が可能であることを証明したことは有名な話である。
ピロリ菌の細菌学的な特徴として、微好気条件下で増殖するグラム陰性菌であり、強力なウレアーゼ活性を示し、尿素をアンモニアに変換することで強酸下での生存を可能にしていることが挙げられる。また、菌形態は、らせん型(spiral
form)と球菌型(cocoid form)をとる。らせん型は鞭毛を持ち、活発な運動性を示すが、球型は代謝活性が低く休止状態にあると考えられている。
ピロリ菌は、感染により急性炎症を胃粘膜に惹起するのみならず、萎縮性胃炎を含む慢性胃炎を形成することにより、消化性潰瘍、胃癌、胃mucosal-associated
lymphoid tissue (MALT) リンパ腫の病態形成に深く関与している。
ピロリ菌の感染率は一般的に発展途上国で高く、先進国で低い。わが国において若年者に感染者は低く、50歳以上になると80%以上の感染率を示すことが報告されている12)。このような感染率の違いは、衛生状態の良し悪しが大きく関与しているものと推察されている。一方、日本を含めたアジアやヨーロッパ数カ国のピロリ菌陽性の胃炎患者の胃粘膜をスコア化された国際的な胃炎分類法で評価して比較した研究では、ヨーロッパ諸国やタイでは腸上皮化生(胃粘膜に小腸上皮が存在する状態)のスコアは低く、日本や中国では腸上皮化生のスコアが高かったという結果が得られている。特にアジア諸国で比較した場合、タイやインドではピロリ菌感染率は高いにもかかわらず、胃がん発生率が低いという調査結果が得られている13)。これらの結果は、感染後の病態の変化が食生活など生活習慣に大きく影響を受けていることを示唆するものであり、とても興味深い。
(2)抗ピロリ菌活性物質
このようなことから、食品に含まれる抗ピロリ菌活性物質の検索に関する研究も数多く進められており、緑茶カテキン類、ガーリック類、クランベリージュース、ブロッコリー、ニンニクなど植物性の食品から多くの抗ピロリ菌活性物質が見出されている14-17)。
一方、動物性食品である乳や乳製品でも抗ピロリ菌活性物質を含むものが見出されている。市販ヨーグルトに利用されている乳酸菌Lactobacillus gasseri LG21をヒトに投与したところ、尿素呼気試験や血中ペプシノゲン1/2比のいずれにおいても統計学上有意な改善が見られている18)。
また、我々は、ピロリ菌の胃受容体への結合を阻止する乳酸菌を発見している19)。乳成分中のラクトフェリンは、in vitroにおいてピロリ菌に対して抗菌活性を示すことが明らかにされている20)。また、乳オリゴ糖であるシアリルラクトースが、ピロリ菌の細胞への付着を阻害することが示されている21)。牛乳自体にも、ピロリ菌感染および萎縮性胃炎を抑制する働きがあることが報告されている22)。この報告では、牛乳を週5回以上摂取している人はピロリ菌感染率が低いことおよび萎縮性胃炎発症率が低いことが報告されており、牛乳の摂取がピロリ菌の感染やその後の病態の変化を抑制すること示唆するものであり、興味が持たれる。このように乳製品における抗ピロリ菌活性を含むものが見出されてきたが、チーズに関する報告は見られない。
(3)抗菌メカニズム
筆者らはこれまで、図3に示したように培養中にピロリ菌の一部の株が自己溶菌を引き起こすという興味深い現象を見出している23)。現在、ピロリ菌の自己溶菌物質を解明している段階にあるが、細胞膜を構成している長鎖脂肪酸であるミリスチン酸(C14:0)が何らかの要因によって放出され、その作用によって細胞膜が溶解することを突き止めている。筆者らの結果は、前項目で述べてきた脂肪酸の抗微生物効果からも強く支持されるものであり非常に興味深いものであった。また、脂肪酸を含むチーズはピロリ菌に対して抗菌作用を示すのではないかということを確信するものであった。
 正常なピロリ菌体 |
 溶菌を引き起こしたピロリ菌体 |
4 チーズ抽出物のピロリ菌に対する抗菌効果
(1)ブルータイプに抗ピロリ菌効果と推定
ブルータイプチーズ3種類、ゴーダチーズ、チェダーチーズおよびプロセスチーズを供試し、各種チーズから水溶性画分とエーテル画分を得て、これらを含む培養液中でピロリ菌を一定時間培養したのちの生残性を検討した。結果は示していないが、いずれのチーズ水溶性画分を含む場合でも、コントロールとほぼ同レベルの菌数が検出され、ほとんど生残性に影響を及ぼさないことが示された。一方、エーテル画分を添加した培地で一定時間保持すると、図4に示したようにブルータイプチーズ由来の試料においては、103cfu/mlから104レベルまで低下しており、この画分に抗菌活性を含む成分が存在することが示唆された。
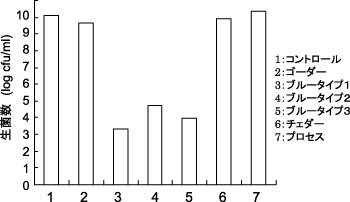
図4 チーズから得られたエーテル画分のピロリ菌の生残性に及ぼす影響
ブルーチーズエーテル抽出物には、ピロリ菌に対する抗菌物質が含まれることが示唆されたことから、エーテル抽出物中に含まれる物質を解析することとした。図5には、6種類のチーズエーテル抽出物を薄層クロマトグラフィーに供した結果を示した。本実験で用いた展開溶媒では、(1)トリアシルグリセロールグループ、(2)脂肪酸グループおよび(3)ジ-アシルグリセロール、モノアシルグリセロールおよびその他の脂質グループ、の3種を大まかに分類できた。特にRf値から矢印で示されたスポットは脂肪酸であると考えられた。供試した6種類のチーズエーテル抽出物の成分を比較すると、ブルータイプチーズにおいて、脂肪酸と推定されるスポットが明確に検出された。さらに、抗菌試験で用いたブルーチーズ1の矢印に相当するスポットを薄層から抽出し、ガスクロマトグラフィーで長鎖脂肪酸の分析条件で定性分析を行った。数種類の脂肪酸が検出され、特にC14:0(ミリスチン酸)、C16:0(パルミチン酸)およびC18:1(オレイン酸)のピークが高く、これらの存在比率が高いことが示唆された。
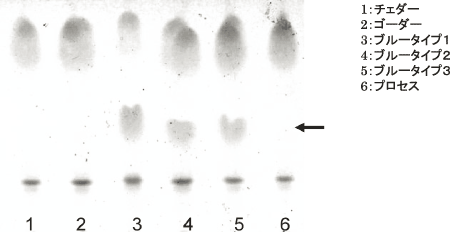
図5 チーズエーテル画分のTLC解析
以上の結果から、ブルータイプチーズのピロリ菌に対する効果は、遊離脂肪酸によるものと推察された。
ブルータイプチーズ中の遊離脂肪酸がピロリ菌の増殖阻害活性を有することが示唆されたことから、標準脂肪酸の増殖に及ぼす影響を検討した。図6には、ピロリ菌の48時間培養時点におけるコントロール(無添加)に対する各種脂肪酸添加培地での生育性を相対吸光度で示した。脂肪酸分子種によって、ピロリ菌の生育性に大きな違いが見られた。すなわち、飽和脂肪酸であるC16:0のパルミチン酸やC18:0のステアリン酸はほとんど生育性に影響を及ぼさなかったが、飽和脂肪酸でも鎖長の短いC14:0のミリスチン酸やC12:0のラウリン酸はピロリ菌の生育を著しく阻害した。また、パルミチン酸やステアリン酸と鎖長が同一であるが不飽和脂肪酸であるオレイン酸やリノール酸もまた顕著な阻害活性を有していた。
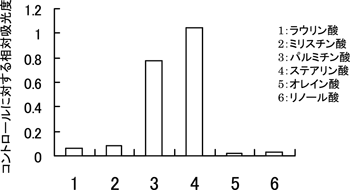
図6 標準脂肪酸がピロリ菌の増殖に及ぼす影響
以上のことから、ブルータイプチーズのピロリ菌に対する抗菌効果は、チーズ中の遊離脂肪酸によるものと結論付けた。
また、標準脂肪酸のピロリ菌に対する抗菌メカニズムを明らかにするため、ミリスチン酸の溶菌メカニズムを検討した。菌懸濁液の菌濃度(OD600)を1.0に調整し、2mMミリスチン酸を添加した際の吸光度の変化を経時的に測定した。図7に示したように、わずか15分で濁度は急激に減少し、未処理の濁度に対して40%以下になった。この結果から、ミリスチン酸はピロリ菌に対して溶菌活性を有していることが明らかになった。
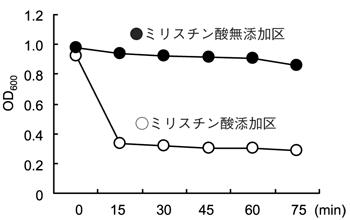
図7 標準脂肪酸がピロリ菌の増殖に及ぼす影響
したがって、ブルーチーズ中の遊離脂肪酸もピロリ菌に対して殺菌的に抗菌効果を示しているものと推察された。
(3)ブルータイプの遊離脂肪酸の溶菌作用と推察
今回、ゴーダー、チェダー、ブルータイプおよびプロセスチーズのピロリ菌に対する抗菌作用を調べたところ、ブルータイプチーズから得られた抽出物に強い抗菌活性が見られた。我々の薄層クロマトグラフィーを用いた実験からは、ブルータイプチーズのみに遊離脂肪酸が検出された。また、標準脂肪酸を用いた実験結果から、供試した脂肪酸の中で、C16:0およびC18:0の脂肪酸以外が、抗ピロリ菌活性を示したことと、それら活性を示した脂肪酸は、ガスクロマトグラフイー分析によって、ブルータイプチーズ中に確実に含まれることが示された。
したがって、ブルータイプチーズ中に含まれる特定の遊離脂肪酸が、抗ピロリ菌活性成分の要因の一つであると推察された。
脂肪酸のピロリ菌の作用機序として溶菌作用によることが示唆された。Thompsonらは、長鎖多価不飽和脂肪酸が抗ピロリ菌活性を示すことを報告しているが、その作用機序として、菌体外膜の流動性を高め、膜の透過性が高まることで小分子の菌体内への流入が起こり、結果として溶菌するのではないかと推察している24)。筆者らの研究では、脂肪酸分子種によって抗菌性の差異が見られた。すなわち、C16:0やC18:0の飽和脂肪酸ではほとんど活性が見られなかったが、飽和脂肪酸であってもC14:0やC12:0では活性が見られ、また、C16:0やC18:0と鎖長が同一であっても不飽和脂肪酸では活性が見られた。これらの理由は全く不明であるが、立体構造上の問題であることは推察される。
おわりに
これまで、チーズ中の抗菌性物質として熟成中に派生してくる乳タンパク由来ペプチドが見出されているが25)、チーズ脂肪酸が抗ピロリ菌活性を持つことを示した例はなく、非常にインパクトのある結果であるといえる。我々の結果は限られたチーズのみでの実験であり、さらにチーズの種類を増やすことで、チーズの抗ピロリ菌作用の全容が明らかにできるであろう。また、作用機序の解明もほとんど進められなかったことから、今後、検討を進めたいと考えている。抗ピロリ菌活性が示されたブルータイプのチーズはし好性の観点からなじみの少ない日本人も多いとも考えられる。
そこで、将来的には、リパーゼ活性の高い乳酸菌のスクリーニングを行い、風味等の改善を図りつつ、より日本人に好まれるピロリ菌活性を示す新しいタイプのチーズの開発を目指したい。
1)堂迫俊一 三次機能 New Food Industry. 2007. 49:47-60.
2)根岸晴夫 チーズの機能 一次機能 New Food Industry. 2008. 50:65-80.
3)井越敬司 チーズの熟成機構 New Food Industry. 2008. 50:48-64.
4)冠木敏秀 チーズ中に含まれるペプチドの生理機能に関する研究 ミルクサイエンス. 2007. 55:157-160.
5)金丸義敏 乳及び乳製品の機能性 −機能性ペプチド− 乳業技術. 2002. 52:11-29.
6)Thormar H, Isaacs CE, Kim KS, Brown HR. Inactivation of visna virus
and other enveloped viruses by free fatty acids and monoglycerides.
Ann N Y Acad Sci. 1994.724:465-471.
7)Sun CQ, O’Connor CJ, Robe AM, The antimicrobial properties of milkfat
after partial hydrolysis by calf pregastric lipase. Chemico-Biological
Interactions. 2002. 140:185-198.
8)Sun CQ, O’Connor CJ, Roberton AM, Antibacterial actions of fatty
acids and monoglycerides against Helicobacter pylori. FEMS Immunology
and Medical Microbiology. 2003. 36:9-17.
9)Sun CQ, O’Connor CJ, MacGibbon AKH, Roberton AM, The products from
lipase-catalysed hydrolysis of bovine milkfat kill Helicobacter pylori
in vitro. FEMS Immunol Med Microbiol. 2007 49: 235-242.
10)Warren, J.R. and Marshall, B.J. Unidentified curved bacilli on
gastric epithelium in active chronic gastritis. Lancet 1983.1273-1275.
11)Marshall, B.J. and Warren, J.R. Unidentified curved bacilli in
the stomachs of patients with gastritis and peptic ulceration. Lancet
1984. 1311-1315.
12)Asaka, M., Kimura, T. and Kato, M. Relationsip of Helicobacter pylori to serum pepsinogen in an asymptomatic Japanese population.
Gastroenterology. 1992. 102:760-766.
13)Liu Y, Ponsioen CI, Xiao SD, Tytgat GN, Ten Kate FJ. Geographic
pathology of Helicobacter pylori gastritis. Helicobacter. 2005. 10:107-113.
14)Lee KM, Yeo M, Choue JS, Jin JH, Park SJ, Cheong JY, Lee KJ, Kim
JH, Hahm KB. Protective mechanism of epigallocatechin-3-gallate against
Helicobacter pylori-induced gastric epithelial cytotoxicity via the
blockage of TLR-4 signaling. Helicobacter. 2004. 9:632-642.
15)Fahey JW, Haristoy X, Dolan PM, Kensler TW, Scholtus I, Stephenson
KK, Talalay P, Lozniewski A. Sulforaphane inhibits extracellular,
intracellular, and antibiotic-resistant strains of Helicobacter pylori
and prevents benzo[a]pyrene-induced stomach tumors. Proc. Natl. Acad.
Sci. U.S.A. 2002. 99:7610-7615.
16)Simon JA, Hudes ES, Perez-Perez GI. Relation of serum ascorbic
acid to Helicobacter pylori serology in US adults: the Third National
Health and Nutrition Examination Survey. J. Am. Coll. Nutr. 2003.
22:283-289.
17)Zhang L, Ma J, Pan K, Go VL, Chen J, You WC. Efficacy of cranberry
juice on Helicobacter pylori infection: a double-blind, randomized
placebo-controlled trial. Helicobacter. 2005. 10:139-145.
18)Sakamoto I, Igarashi M, Kimura K, Takagi A, Miwa T, Koga Y. Suppressive
effect of Lactobacillus gasseri OLL 2716 (LG21) on Helicobacter pylori
infection in humans. J. Antimicrob. Chemother. 2001. 47:709-710.
19)Mukai T, Asasaka T, Sato E, Mori K, Matsumoto M, Ohori H. Inhibition
of binding of Helicobacter pylori to the glycolipid receptors by
probiotic Lactobacillus reuteri. FEMS Immunol. Med. Microbiol. 2002.
32:105-110.
20)Nakao K, Imoto I, Ikemura N, Shibata T, Takaji S, Taguchi Y, Misaki
M, Yamauchi K, Yamazaki N. Relation of lactoferrin levels in gastric
mucosa with Helicobacter pylori infection and with the degree of
gastric inflammation. Am. J. Gastroenterol. 1997 92:1005-1011.
21)Simon PM, Goode PL, Mobasseri A, Zopf D. Inhibition of Helicobacter pylori binding to gastrointestinal epithelial cells by sialic acid-containing
oligosaccharides. Infect. Immun. 1997. 65:750-757.
22)Akedo I, Tatsuta M, Narahara H, Iishi H, Uedo N, Yano H, Ishihara
R, Higashino K, Ishida T, Takemura K, Matsumoto S. Prevention by
bovine milk against Helicobacter pylori-associated atrophic gastritis
through its adherence inhibition. Hepatogastroenterology. 2004. 51:277-281.
23)Fujita Y, Yamaguchi K, Kamegaya T, Sato H, Semura K, Mutoh K,
Kashimoto T, Ohori H, Mukai T. A novel mechanism of autolysis in
Helicobacter pylori: possible involvement of peptidergic substances.
Helicobacter 2005. 10:567-576.
24)Thompson L, Cockayne A, Spiller RC. Inhibitory effect of polyunsaturated
fatty acids on the growth of Helicobacter pylori: a possible explanation
of the effect of diet on peptic ulceration. Gut 1994. 35:1557-1561.
25)Rizzello CG, Losito I, Gobbetti M, Carbonara T, De Bari MD, Zambonin
PG. Antibacterial activities of peptides from the water-soluble extracts
of Italian cheese varieties. J. Dairy Sci. 2005. 88:2348-2360.
26)Ogawa J, Kishino S, Ando A, Sugimoto S, Mihara K, Shimizu S. Production
of conjugated fatty acids by lactic acid bacteria. J Biosci Bioeng.
2005 100:355-364